
El misterioso caso de la aterosclerosis.
José Davidow
28 ene 2026
Saber o no saber, esa es la cuestión.
Cuanto sabemos y cuanto no sabemos, sobre el mayor azote de la humanidad, la enfermedad de las arterias. La aterosclerosis. La principal causa de muerte en el mundo.
De inmediato, al preguntarnos, ya creemos tenemos la respuesta, es el colesterol. La molécula maldita. Por ella morimos.
Pero sin ella no vivimos. Un cuerpo adulto tiene alrededor de 100 gramos de colesterol, distribuido en las membranas celulares, otras estructuras y moléculas. Componente esencial para la vida, está presente en todas las células del cuerpo y en muchas hormonas, así como en la vitamina D.
¿Podrían ser otras las causas de la aterosclerosis? ¿O es un caso cerrado? Para numerosos médicos y casi todas las personas, es caso cerrado. El maldito colesterol, las grasas. Y el remedio supremo, las estatinas
La enfermedad cardiovascular es la causa principal de muerte en el mundo entero y la aterosclerosis es su causa determinante. Aunque existen avances en su prevención y tratamiento, parecería que queda mucho por hacer. En especial en las etapas tempranas y asintomáticas de la enfermedad.
Existe consenso en que la aterosclerosis es una enfermedad compleja y multifactorial, asi dicen todos. Yo detesto la palabra, multifactorial, siempre aparece para esconder la ignorancia.
Su prevención y tratamiento está centrada en eliminar algunos factores, “de riesgo”, como el fumar, y un factor único que se considera esencial, el colesterol elevado.
Bajar los niveles de colesterol, es la terapia utilizada habitualmente para prevenir el inicio y el progreso de la aterosclerosis.
Muchos pacientes, con el tratamiento considerado óptimo en la actualidad, siguen teniendo riesgo alto. (Nelson K, Fuster V, Ridker PM., 2023) (1) (Kaasenbrood L, Boekholdt SM, et al., 2016) (2)
La respuesta habitual a ese riesgo, es insistir en valores cada vez más bajos de colesterol LDL.
Se ha postulado la la posible existencia de otros factores, que pudieran intervenir en el proceso aterosclerótico. En especial en la población que, con los actuales tratamientos, sigue teniendo un riesgo residual importante. Que es mayoría. Y así también en la población aparentemente sana, identificando tempranamente a quienes puedan estar en riesgo. (Libby P., 2020) (3)
En este post pondremos al colesterol en pausa, para explorar otras alternativas en relación a la aterosclerosis.
Antes de ponerlo en pausa recordemos algo del colesterol.
El colesterol es un lípido (del tipo esterol) que se encuentra en la membrana plasmática eucariota, los tejidos corporales de todos los animales y en el plasma sanguíneo de los vertebrados. Pese a que las cifras elevadas de colesterol en la sangre tienen consecuencias perjudiciales para la salud, es una sustancia estructural esencial para la membrana plasmática. Abunda en las grasas de origen animal.
François Poulletier de la Salle, identificó por primera vez el colesterol en forma sólida en los cálculos de la vesícula biliar en 1769. Sin embargo, fue en 1815 cuando el químico Michel Eugène Chevreul nombró el compuesto «colesterina», del griego χολή, kolé, ‘bilis’ y στερεος, stereos, ‘sólido’.
La biosíntesis del colesterol tiene lugar en el retículo endoplasmático liso de prácticamente todas las células de los animales vertebrados.
La producción en el humano es regulada directamente por la concentración del colesterol presente en el retículo endoplásmico de las células, habiendo una relación indirecta con los niveles plasmáticos de colesterol presente en las lipoproteínas de baja densidad (LDL por su acrónimo inglés). Una alta ingesta de colesterol en los alimentos conduce a una disminución neta de la producción endógena y viceversa. (de Wikipedia, 9-09-25)
Si bien se evalúan actualmente, factores diversos entre las causas de la aterosclerosis, desde inflamatorios, a mutaciones de las células madre de la médula ósea, generando una hematopoyesis clonal, en este post vamos a prestar atención al microbioma. (Libby P.,2020). (3)
El microbioma intestinal está de moda. Todos los padecimientos humanos parecen relacionarse con el mismo. Algunas de estas especulaciones pueden ser ciertas.
Un nuevo jugador: el Microbioma o Microbiota.
El intestino humano alberga un complejo y diverso sistema de microorganismos, consistente en bacterias, hongos, virus, archae y protozoos.
Este ecosistema contribuye a un gran número de funciones necesarias, la fermentación de los componentes no digeribles de la dieta, la síntesis de vitaminas, las defensas contra bacterias patógenas, la maduración de las defensas inmunológicas, el mantenimiento de la barrera intestinal.
Se ha calificado al intestino y su microbioma como “el segundo cerebro” dadas sus funciones y rol significativo en la fisiología y la homeostasis. Las especies que albergamos en el intestino producen numerosos metabolitos a partir de los componentes de la dieta. O resultantes de su propia actividad.
Estos metabolitos, estas sustancias químicas, son parte esencial de un diálogo entre microbiota y su huésped. Ingresan en la circulación y se asocian con beneficios para la salud y también con diversas enfermedades.
Hay evidencias de que influyen en múltiples padecimientos, como la diabetes, las enfermedades reumáticas, la enfermedad cardiovascular, la hipertensión, y la aterosclerosis que es nuestro tema de hoy. (Tang WH, Wang Z, Levison BS., et al 2013) (4) (Agus A, Clément K, Sokol H., 2021) (5)
Mencionemos algunas características del microbioma humano.
Microbioma intestinal. El intestino de un humano adulto alberga algo así como 4 trillones de microorganismos. Se denomina microbioma intestinal, microbiota, flora bacteriana o flora intestinal al conjunto de microorganismos (bacterias, virus y hongos) que viven en el intestino, en una relación de simbiosis tanto de tipo comensal como de mutualismo. Se calcula que el ser humano tiene en su interior unas dos mil especies bacterianas diferentes, de las cuales solamente cien pueden llegar a ser perjudiciales.
En términos taxonómicos, las bacterias se organizan en varios niveles jerárquicos. En la cúspide de esta clasificación se encuentran los filos, que agrupan bacterias con características estructurales y funcionales comunes. Los filos se dividen en géneros, y estos en especies.
Los filos bacterianos en el intestino humano son Bacillota (Firmicutes), Bacteroidetes, Actinomicetos y Pseudomonadota.
La mayoría de las bacterias pertenecen a los géneros Bacteroides, Clostridium, Faecalibacterium, Eubacterium, Ruminococcus, Peptostreptococcus, Peptococcus y Bifidobacterium. Las especies del género Bacteroides constituyen el 30%, sugiriendo que este grupo es especialmente importante para el huésped.
Los géneros de hongos detectados en el intestino incluyen Cándida, Saccharomyces, Aspergillus, Penicillium, Rhodotorula, Trametes, Pleospora, y otros.
Se conoce poco sobre el viroma del intestino humano, excepto los conocidos patógenos que pueden atacarnos, como los enterovirus, rotavirus, norovirus y otros.
En los últimos años se ha comenzado a valorar el rol del ecosistema microbiano intestinal. una idea augurada por Metchnikoff en el siglo XIX. Los avances en la biología molecular, la genómica y la metabolómica, han permitido comprender con mayor claridad la relación entre ese ecosistema y la salud de su huésped. Un microbioma saludable apoya las funciones metabólicas vitales, sostiene la integridad de la barrera intestinal, optimiza la extracción de energía, protege de los patógenos y modula el sistema inmune.
El microbioma actúa como un intermediario entre el huésped y su dieta, produciendo diversos metabolitos, sustancias bioactivas, que previamente modificadas por las enzimas del huésped pueden ser valiosas o promover enfermedades.
La dieta de las sociedades modernas, con sus alimentos procesados, carencia de fibra, de antioxidantes y de bacterias benéficas, favorecen un microbioma productor de sustancias que influyen en diversas enfermedades.
Merecen especial atención como causantes de enfermedad, dos de ellas: el TMAO, y el Imidazol Propionato. Muchas publicaciones se refieren a estas sustancias. Se destacan entre las numerosas que se producen en la interacción de los alimentos y las bacterias.
TMAO, trimetilamina oxidada.
Uno de los metabolitos que se generan en el intestino, es la trimetilamina. Deriva de la acción bacteriana sobre la fosfatidilcolina, colina y carnitina de la dieta, que abundan en los alimentos de origen animal, (Tang WH, Wang Z, Levison BS, et al., 2013) (4)
Juega un rol en la patogenia de varias enfermedades al ser oxidada. Los precursores de trimetilamina abundan en las dietas omnívoras, que incluyen carnes, huevos, pescado de mar y lácteos.
Esos nutrientes son convertidos por el microbioma en trimetilamina, que absorbida, pasa al hígado y es transformada en TMAO, trimetilamina oxidada, por la enzima FMO3, (flavin containing monooxygenase 3).
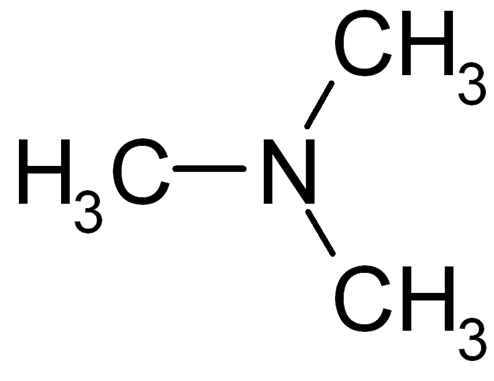
Trimetilamina.
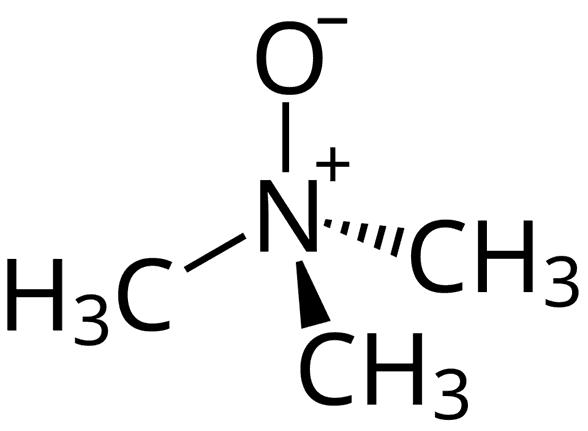
Trimetilamina oxidada. TMAO.
La carnitina, es una trimetilamina y abunda en la carne roja. Se ha demostrado que produce aterosclerosis en ratones.
En varios modelos animales TMAO, promueve el desarrollo de aterosclerosis. Genera un medio interno propicio a las trombosis. Es por lo tanto un factor de elevado riesgo en pacientes con aterosclerosis coronaria y cerebral, favoreciendo el infarto de miocardio y el ACV.
El nivel plasmático de TMAO, se asocia con enfermedad cardiovascular en estudios clínicos y de poblaciones. Aumenta la incidencia aterosclerosis y la trombosis en diversos estudios. (Agus A, Clément K, Sokol H et al., 2021) (5) (Zhu W, Gregory JC, Org E, et al. 2016) (6)
Los niveles plasmáticos de L-carnitina en sujetos sometidos a evaluación cardiovascular, y con altos niveles de TMAO, predicen riesgo aumentado de enfermedad y eventos cardíacos, infartos, ACV y muerte, (Liu W, Wang L, Ou J, et al., 2025) (7) (Koeth RA, Wang Z, Levison BS., et al., 2013) (8)
TMAO contribuye a generar hiperglucemia e intolerancia a la glucosa. Por este mecanismo agravaría la evolución de las lesiones arteriales, y las complicaciones del síndrome metabólico. (Chen S, Henderson A, Petriello MC. Et al., 2019) (9) (Agus A, Clément Sokol H. 2021) (5)
En pacientes con enfermedades cardiometabólicas o renales crónicas, niveles elevados de TMAO, se asocian con mayor mortalidad por todas las causas. (Haghikia A, Li XS et al 2019) (10), (Wang M, Li XS, Wang Z, de Oliveira Otto MC, et al., 2023) (11)
En esta última publicación, que incluyó 6785 adultos del Estudio Multiétnico de la Aterosclerosis, (Multi-Ethnic Study of Atherosclerosis), TMAO fue medida al comienzo y a los 5 años. Se evaluó la mortalidad por todas las causas y la enfermedad cardiovascular, durante un seguimiento de 16 años. La conclusión fue que los niveles de TMAO elevados, se correlacionaron con la mortalidad, especialmente las muertes por enfermedad cardiovascular y enfermedades renales.
Un estudio sobre alimentación y producción de TMAO, compara el consumo de carnes rojas, carnes blancas, o proteínas vegetales y llega a la siguiente conclusión: “… el consumo de carnes rojas incrementa los niveles sistémicos de TMAO, a través del aumento de los precursores dietéticos, la producción aumentada de TMAO a partir de carnitina y la reducción de la excreción renal de TMAO. Al suprimir la carne roja el nivel de TMAO, se normaliza en 4 semanas”. (Wang Z, Bergeron N, Levison BS., et al., 2019) (12)
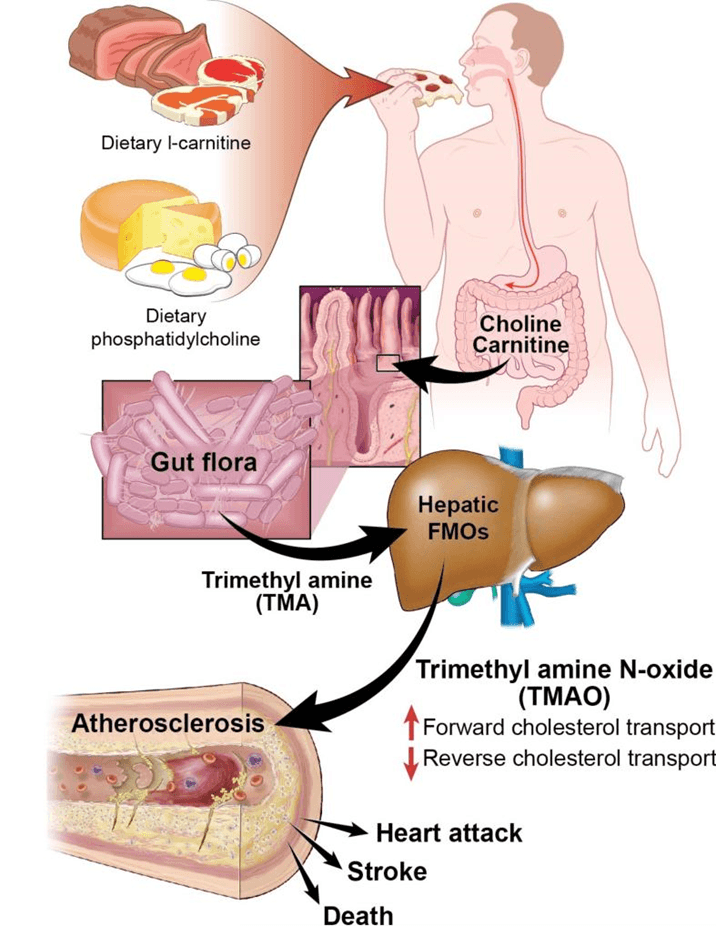
Efectos de TMAO. Tomado de Brown JM, Hazen SL. Metaorganismal nutrient metabolism as a basis of cardiovascular disease. Curr Opin Lipidol. 2014. (15)
Imidazol Propionato.
El propionato de imidazol (ImP), es un metabolito proinflamatorio creado por las bacterias intestinales a partir de la histidina.
Del ImP sabemos hoy que está vinculado fuertemente a la aterosclerosis, actuando como marcador de riesgo y diana terapéutica, y afectando el metabolismo de la glucosa y la función endotelial;
Inicialmente fue descubierto en pacientes con inflamación intestinal, en 1972, por Van der Heiden C, Wadman SK, et al. Observaron que se asociaba a este padecimiento y que estaba ausente en la materia fecal y en la orina de personas sanas. (Van der Heiden C, Wadman SK, et al., 1972) (13)
Durante muchos años el interés en esta sustancia desaparece, hasta que, en el 2018, investigadores en Suecia, descubrieron su asociación con la resistencia a la insulina, en ratones y humanos, generando nuevo interés en esta molécula. (Koh A, Molinaro A, Ståhlman X, et al., 2018) (14)
Luego diversos estudios clínicos revelaron la relación estrecha entre los niveles circulantes de ImP y trastornos metabólicos y enfermedad cardiovascular, diabetes tipo 2, hipertensión, obesidad, aterosclerosis, insuficiencia cardíaca y otros padecimientos. (Molinaro A, Bel Lassen P, et al.,2020) (16)
El imidazol propionato, denominado, además, como dihidrourocanato, o dIaminohistidina, se origina por la actividad del microbioma sobre el aminoácido histidina.
La histidina es un aminoácido esencial, que se obtiene de la dieta. Sustrato fundamental en la síntesis de proteínas y precursor de la histamina, que se forma por la acción de la histidina decarboxilasa.
La histidina no utilizada en estas funciones, es convertida en trans-urocanato por la histidina-amonio liasa. Subsecuentemente pasa a cis-urocanato en la piel y a glutamato y amonio en el hígado.
En el colon el trans-urocanato es transformado por las bacterias en imidazol propionato.
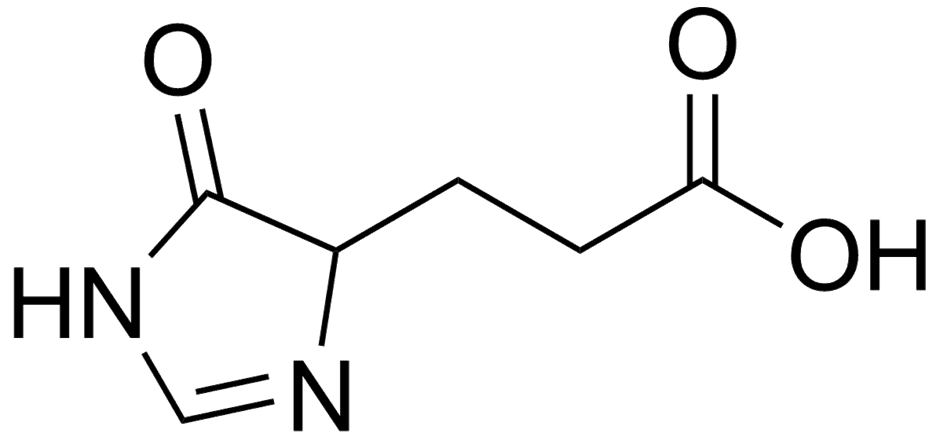
Ácido trans-urocánico.
El ácido trans-urocánico (trans-UCA) es un compuesto natural en la piel, derivado de la histidina, que absorbe la luz UV y se convierte en su isómero cis con la exposición solar, jugando un rol clave en la protección solar y la respuesta inmune, con potenciales aplicaciones dermatológicas como antioxidante y modulador inmunitario, y es un metabolito importante en el catabolismo de la histidina.
En condiciones fisiológicas los niveles de ImP varían poco en el individuo y son muy bajas. En condiciones patológicas como la diabetes y la enfermedad cardiovascular las concentraciones aumentan hasta cien veces.
A pesar de derivar del metabolismo de la histidina, estos niveles no dependen tanto del consumo de histidina, sino de la actividad enzimática y la composición del microbioma intestinal. (Molinaro A, Bel Lassen P, et al., 2020) (16)
La reductasa del urocanato UrdA, es la responsable de la producción de ImP y está presente en algunos tipos de bacterias del microbioma.
Las bacterias asociadas a este efecto son entre otras: Streptococcus mutans, Eggerthella lenta, Clostridium symbiosum, Pseudoflavonifractor, Eubacterium eligens, Ruminococcus gnavus. Aerococcus urinae, Anaerococcus prevotii, por citar algunas.
ImP y diabetes.
Un aumento en la circulación portal y sistémica de imidazol propionato, se observa en pacientes con diabetes, en comparación con personas no diabéticas. Administrado a ratones, el imidazol propionato induce resistencia a la insulina y glucemias elevadas. Atenúa el efecto sobre la glucemia de la metformina.
Estudios epidemiológicos han demostrado una correlación muy robusta entre los niveles de ImP y el desarrollo de resistencia a la insulina, diabetes, inflamación crónica y alteración de la barrera intestinal.
ImP y otras enfermedades.
Asimismo, ImP se observa elevado, en la enfermedad renal crónica, la progresión de la aterosclerosis y la mortalidad en la insuficiencia cardíaca.
Ver (Hua S, Lv B, Qiu Z., et al. 2023) (17) (Zeng Y, Wu Q, Guo M, et al., 2025) (18) (Xu Q, Wang W, Li Y, Liu Y and Liu Y, 2024) (19)
El estudio METACARDIS, ha sido un proyecto de amplia escala europeo (Metagenomics in Cardiometabolic Diseases), que investigó el rol del microbioma intestinal en las enfermedades cardiometabólicas: obesidad, diabetes y enfermedad cardiovascular.
Su objetivo ha sido desarrollar aproximaciones diagnósticas y terapéuticas para estos padecimientos utilizando metagenómica para comprender la relación entre la flora intestinal, el genoma del huésped y la enfermedad.
En un sub análisis de este estudio, que incluyó participantes con enfermedad cardiovascular isquémica, se reveló la presencia de elevados niveles de ImP en estas personas. Se demostró una fuerte correlación positiva entre el nivel de ImP y marcadores de inflamación, incluyendo el recuento de leucocitos, proteína C reactiva de alta sensibilidad y CXCL10.
Esta última, también llamada: proteína inducida por el interferón gamma 10 (IP-10), es una citoquina que juega un importante papel en la respuesta inflamatoria. (Fromentin, S., Forslund, S.K., Chechi, K. et al., 2022) (20)
Recientemente Molinaro et al., investigaron la asociación de niveles circulantes de ImP, insuficiencia cardíaca y mortalidad. Midieron los niveles de ImP en dos cohortes independientes de paciente, Una europea, con 1985 personas y otra en EEUU, con 2.155. En ambas pacientes con grados variables de enfermedad cardiovascular.
Niveles elevados de ImP se observaron en individuos con enfermedad cardiovascular y personas con insuficiencia cardíaca, comparando con sujetos sin dichas patologías. Los niveles más altos de observan en los pacientes con insuficiencia cardíaca.
Los niveles de ImP se asociaron inversamente con la fracción de eyección, y positivamente con el valor del péptido natriurético atrial (pro- ANP) y el (NT-pro-BNP) en ambas cohortes.
El seguimiento reveló que los niveles más elevados de ImP, se asociaron con un aumento de la mortalidad, aun ajustando con los factores de riesgo tradicionales.
“…ImP es un predictor significativo e independiente de mortalidad a 5 años”. (Molinaro A, Nemet I, Bel Lassen P, et al., 2023) (23
Dos recientes publicaciones, una en julio del 2025, en Nature, de Annalaura Mastrangelo, Iñaki Robles-Vera, et al. “Imidazole propionate is a driver and therapeutic target in atherosclerosis. Nature 645, 254–261 (2025). (21)
Y otra, en mayo del 2025, de Vanasa Nageswaran, Alba Carreras, Leander Reinshagen et al., en Arterioscler Thromb Vasc Biol. 2025, (22) Hacen una evaluación similar del papel de ImP.
Me han parecido de gran importancia. Voy a señalar algunos aspectos.
Primer estudio.
El de Mastrangelo Robles Vera, et al. Fue conducido en el Centro Nacional Español para la Investigación Cardiovascular, (CNIC) y financiado por el Consejo Europeo de Investigaciones. Los autores identifican al imidazol propionato (ImP), como un agente promotor de aterosclerosis. Afirman que los niveles de ImP constituyen un marcador diagnóstico temprano. Su presencia en la sangre se asocia con el desarrollo de aterosclerosis en personas aparentemente sanas. Y abre posibilidades de nuevos tratamientos.
La publicación expresa en la introducción: “Aquí observamos que el Imidazol Propionato, producido por el microbioma intestinal, se asocia con aterosclerosis en roedores y en dos cohortes humanas independientes. Además, la administración de ImP a ratones propensos a desarrollar aterosclerosis, fue suficiente para inducir aterosclerosis, sin modificar el perfil lipídico. Esto se asoció con la activación de la inmunidad innata y adaptativa y la inflamación en forma local y sistémica.
Esta investigación incluyó, además, a 400 voluntarios humanos del estudio PESA (Progression of Early Subclinical Atherosclerosis), una cohorte prospectiva del Centro de investigaciones Cardiovasculares de Santander, España. Se realizaron estudios de imágenes multimodales y multiterritoriales, tomográficas y ecográficas.
Esto permitió clasificar a 295 participantes como afectados por aterosclerosis subclínica y 105 controles sanos. Los niveles de ImP, pero no de histidina o ácido urocánico, se mostraron elevados en las personas afectadas y no en los controles. Se observó una relación lineal entre la concentración de ImP y la aterosclerosis y una relación no lineal con la extensión de la aterosclerosis.
ImP parece superior, para discriminar la presencia de aterosclerosis activa, a los niveles de LDL y Proteína-C reactiva.
Esto sugiere su uso potencial como indicador de aterosclerosis activa antes de que ocurran otras comorbilidades.
Además, dicen los autores: “…Específicamente encontramos que ImP produce aterosclerosis actuando sobre el receptor Imidazolina-1, (I1R también conocido como Nischarina), en las células mieloides.
Bloqueando este eje ImP-I1R se inhibe el desarrollo de aterosclerosis, inducida por ImP o por una dieta elevada en colesterol. La identificación de la fuerte asociación de ImP con la aterosclerosis activa y su contribución al progreso de la enfermedad abre nuevas posibilidades para el diagnóstico temprano y el tratamiento”.
Nischarina es una proteína que en humanos es codificada por el gen NISCH. Está involucrada en la regulación de varias vías de señalamiento, incluyendo las relacionadas con supervivencia celular, migración y crecimiento de tumores. Funciona interactuando con otras proteínas como las RabGTPasas, y proteínas LRR. (Wikipedia,.9-12-25)
En la Discusión agregan: “…Demostramos que ImP induce aterosclerosis sin influenciar los valores de colesterol. Los efectos pro aterogénicos de ImP pueden ser pleiotrópicos y actuar sobre múltiples tipos celulares. Observamos que la administración de ImP induce un aumento de la actividad de transcripción de macrófagos, fibroblastos y en menor cuantía, células endoteliales. Estos cambios se caracterizan por un aumento del reclutamiento de células de la inmunidad e inflamación que explicarían el efecto proaterogénico. Además, ImP activa las respuestas aterogénicas sistémicas innatas y adaptativas que llevan a un aumento de la infiltración de células inmunes en las raíces aórticas, contribuyendo al progreso de la aterosclerosis”.
El estudio demuestra que el bloqueo del receptor I1R, en modelos animales, previene la formación de placas, aun cuando los animales son alimentados con una dieta alta en colesterol.(Mastrangelo, A., Robles-Vera, I., Mañanes, D. et al., 2025) (21)
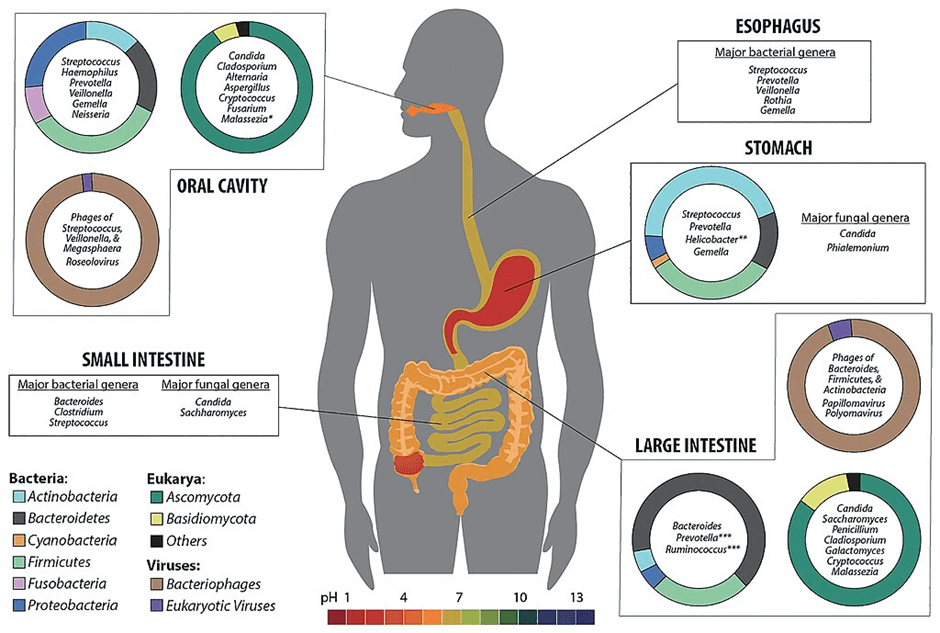
Microbioma humano. Ethan Hillman et al. Wikimedia Commons.
Segundo estudio.
El de Vanasa Nageswaran, Alba Carreras, Leander Reinshagen et al., se examina también el papel de ImP, en la enfermedad cardiovascular.
Así lo expresan: “… en este estudio buscamos determinar la asociación entre los niveles de ImP en la circulación y el riesgo de enfermedad coronaria en humanos. Exploramos el rol de ImP en el desarrollo de aterosclerosis en roedores. Investigamos los efectos de niveles elevados de ImP en el funcionamiento del endotelio, y el impacto en la capacidad de reparación del mismo.
Concluyen:
“…Los niveles elevados de imidazol propionato se asocian con un aumento de la prevalencia de la enfermedad coronaria en humanos, aún después de ajustar los datos a los factores de riesgo tradicionales. Además, evidenciamos que ImP contribuye en forma causal al desarrollo de aterosclerosis, al alterar los mecanismos que protegen los endotelios vasculares. En modelos in vitro e in vivo, ImP acelera el desarrollo de la aterosclerosis y por lo tanto de la enfermedad cardiovascular.
“…Actuar sobre los mecanismos de producción de ImP, o bloquear estos efectos, constituyen un concepto nuevo en la prevención de la enfermedad cardiovascular.” (Nageswaran V, Carreras A, Reinshagen L, Beck KR, et al. 2025) (22)
Adenda.
Y la enfermedad de Parkinson. ¿También.?
Una reciente publicación en Nature, en septiembre del 2025, de Hyunji Park, Jiwon Cheon, et al., relaciona la producción de ImP, con la enfermedad de Parkinson.
Dicen en la Introducción: “… Demostramos que niveles elevados de Streptococcus Mutans y su enzima urocanato reductasa (UrdA), que produce imidazol propionato, están presentes en el microbioma de pacientes con enfermedad de Parkinson, junto con niveles elevados de ImP en el plasma.
Este metabolito llega al cerebro y produce neurodegeneración…La colonización de ratones con Streptococcus Mutans productor de UrdA, aumenta los niveles sistémicos y cerebrales de ImP, induciendo síntomas de Parkinson, pérdida de neuronas dopaminérgicas, astrogliosis, microgliosis y síntomas motores de Parkinson.
La administración de ImP recapitula las manifestaciones principales del Parkinson”. (Park H, Cheon J, Kim H, Kim J, Kim J, et al., 2025) (24)
Progreso del conocimiento. Se encuentren causas. Insisto en detestar afirmaciones tales como: “el origen es policausal”, o “factores genéticos y ambientales.”. O nuestros famosos, (de los médicos), Idiopático, o criptogenético, con lo que parecemos decir algo inteligente. Prefiero “de causa desconocida”.
Ante nuevas perspectivas. Los verdaderos drivers de la aterosclerosis y los nuevos blancos terapéuticos.
Los estudios referidos hacen pensar que no es el colesterol la causa primaria, de la aterosclerosis, aunque contribuya, cuando está elevado, a su evolución. Por largo tiempo se ha discutido su papel, causa primaria o concomitante del desdichado proceso que mata a la mayoría de las personas. Los hallazgos referidos en estas líneas apuntan a causas más básicas.
Entonces, debemos pensar en cómo reducir los niveles de ImP y TMAO. Y tal vez otros productos del microbioma. Que podrían ser los motores reales de la aterosclerosis.
La dieta actual, en el mundo desarrollado, se caracteriza por el bajo nivel de fibra y al alto nivel de proteínas animales, grasas saturadas y azúcares. Esta dieta se ha relacionado fuertemente con enfermedades cardiometabólicas. (Clemente-Suárez VJ, et al. 2023) (25)
Por el contrario, las dietas que pueden catalogarse dentro de ese espectro llamado “Dieta Mediterránea”, o la vegetariana, que abundan en proteína vegetal, han demostrado beneficios metabólicos. (Threapleton DE, Greenwood DC, et al 2013) (26)
El consumo de fibra y la adherencia a un patrón dietético “saludable” se correlaciona con disminución de la resistencia a la insulina, y la aparición de diabetes, probablemente al reducir los niveles de ImP y de TMAO.
Estas dietas altas en fibra, de frutas y vegetales, se asocian con un microbioma intestinal más variado, diverso.
En el estudio Meta Cardis, los niveles circulantes de ImP, se correlacionaron positivamente con el consumo de proteínas y grasas saturadas y negativamente con el consumo de grasas no saturadas y fibra, de vegetales y frutos secos. (Molinaro A, Bel Lassen P, et al., 2020) (16)
En una intervención que duró dos semanas que involucró sujetos sanos, el cambio de la dieta Western, a una rica en fibra, frutas, vegetales y proteínas, demostró un franca disminución de la presencia de ImP en la orina. (Wellington N, Shanmuganathan M, et al., 2019) (26)
Creer o no creer, that is the question.
Darle o no importancia al microbioma y su influencia en la aterosclerosis, esa parece ser la cuestión. O apegarse a la idea de los factores de riesgo tradicionales.
O al único importante, según la opinión general, la creencia general, la moda de la época: el colesterol LDL elevado.
La teoría de los 7 países, del héroe, (o villano), Ancel Keys, concluye que la dieta mediterránea protege de la enfermedad coronaria por ser baja en grasas saturadas.
La obsesión de Keys, era que las grasas saturadas de la dieta occidental, elevaban el colesterol y causaban la aterosclerosis. Su estudio ha sido acusado de “Cherry picking”, elegir los países que dan la razón a su idea y dejar de lado otros, con dietas ricas en grasas saturadas y bajos niveles de enfermedad aterosclerótica.
Veámoslo de otra manera.
La dieta mediterránea es baja en grasas saturadas y colesterol. A esa condición Ancel Keys le atribuía sus ventajas.
Pero es a su vez la dieta que disminuye la producción de ImP y TMAO por el microbioma.
Para disminuir los niveles circulantes de TMAO (trimetilamina N-óxido), es importante:
Reducir el consumo de precursores de TMAO, que aumentan su producción. Los principales precursores son colina, carnitina y betaína, abundantes en:
Carne roja (especialmente vacuno, cordero)
Vísceras (hígado, riñón)
Yema de huevo (alto en colina)
Embutidos y carnes procesadas
Lácteos enteros (leche, quesos)
Pescados y mariscos (especialmente los de agua fría: caballa, salmón, atún, sardina, gambas, mejillones…). Aunque el pescado aumenta TMAO agudamente, a largo plazo es cardioprotector por otros mecanismos.
Adoptar una dieta predominantemente basada en plantas (vegetariana, o mediterránea con poca carne roja) reduce TMAO entre 30-60% en semanas. (Wang Z, Bergeron N, Levison BS., et al., 2019) (12)
Para reducir imP.
El ácido imidazol-propiónico (ImP) es un derivado del metabolismo bacteriano de la histidina. La histidina es un aminoácido esencial, no podemos prescindir de la histidina.
Una dieta que reduce la producción de ácido imidazol-propiónico (ImP) por el microbioma intestinal se centra principalmente en reducir los sustratos que alimentan a las bacterias productoras de ImP.
Se ha sugerido que no es la cantidad de histidina de la dieta lo prioritario, sino las bacterias intestinales que la generan. Para ello sería importante la dieta rica en fibra y los probióticos (yogurt, chucrut, kimchi). (Molinaro A, Bel Lassen P. et al., 2020)
Alimentos muy ricos en histidina:
Vísceras (hígado, riñones, sesos, mollejas)
Carnes rojas y caza
Mariscos (gambas, mejillones, vieiras,
Pescados azules (caballa, sardina, anchoas, salmón, atún)
Alimentos moderados en histidina:
Carnes blancas (pollo, pavo)
Pescado blanco (merluza, bacalao, lenguado)
Legumbres.
Adoptar un enfoque centrado en la salud intestinal, similar a una dieta mediterránea, es la mejor estrategia para reducir los niveles de este metabolito, el ImP. (Wellington N, Shanmuganathan M, de Souza RJ, et al., 2019) (27)
Otros Factores Clave. Para la salud intestinal y general.
Además de la dieta, el estilo de vida influye significativamente:
Ejercicio físico: La actividad física regular mejora la diversidad y cantidad de bacterias intestinales beneficiosas.
Manejo del estrés: El estrés crónico afecta la conexión cerebro-intestino y puede dañar el microbioma.
Sueño adecuado: Dormir lo suficiente es esencial para la salud intestinal.
Suplementación: Se ha observado que suplementar con magnesio puede ayudar a reducir la producción de propionato de imidazol por el microbioma. (Fan L, Yu D, Zhu X, Huang X, et al., 2021) (28)
Conclusiones.
Entonces, de seguir confirmándose estos estudios, el colesterol dejará de ser lo más importante. Se considerarán otros mecanismos causales, independientes del colesterol.
El microbioma y sus metabolitos derivados, son significativos. Como señalan Annalaura Mastrangelo e Ignacio Robles-Vera, “…Demostramos que ImP induce aterosclerosis sin influenciar los valores de colesterol. Los efectos pro aterogénicos de ImP pueden ser pleiotrópicos y actuar sobre múltiples tipos celulares.
…ImP activa las respuestas aterogénicas sistémicas innatas y adaptativas que llevan a un aumento de la infiltración de células inmunes en las arterias, contribuyendo al progreso de la aterosclerosis”. (Mastrangelo, A., Robles-Vera, I., Mañanes, D. et al., 2025) (21)
Un comentario de Iñaki Robles Vera, coautor del estudio dice; “ No solo observamos niveles elevados de ImP en personas con aterosclerosis, demostramos que ImP es un agente causal de la enfermedad. En modelos animales de aterosclerosis la administración de ImP lleva a la formación de placas arteriales. Lo hace activando el receptor de imidazolina tipo 1 (I1R), incrementando así la inflamación sistémica y promoviendo la aterosclerosis.”
Componentes de la dieta son el origen, el agente mediador el microbioma, y los metabolitos dañan las arterias. El colesterol se agrega luego a la pared dañada.
Algo de la opinión de Keys era cierto. La dieta mediterránea es útil. Con el correr del tiempo habrá medicamentos que protejan de TMAO y de ImP.
Mucho queda por descubrir en el misterio de la aterosclerosis.

Centro Nacional Español para la Investigación Cardiovascular, (CNIC) El grupo de trabajo.
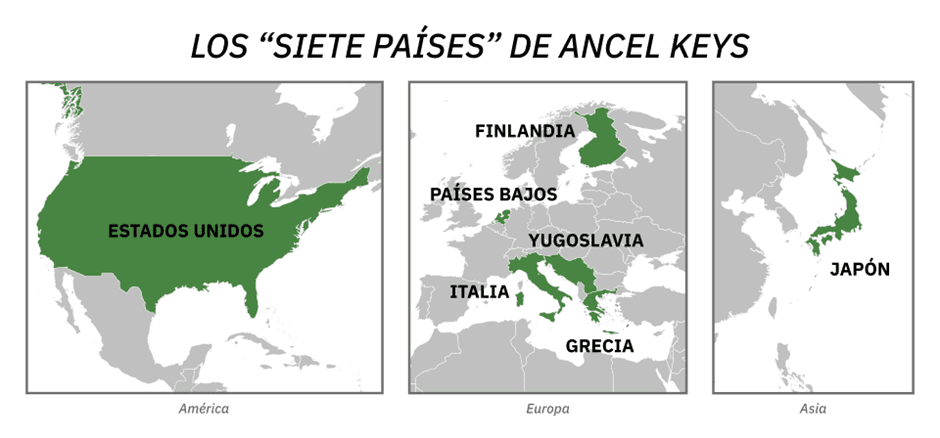
Los siete países estudiados por Ancel Keys, de “El moro español”, Wikimedia Commons.
REFERENCIAS
To add a video to your site, click the “Insert” button and navigate to the “Media” section. Then, drag and drop a video component onto the Canvas.